Oteste da cannabis medicinal finalmente começou. Na sexta-feira, 26 de março de 2021, a planta medicinal foi prescrita pela primeira vez no Hospital Universitário de Clermont-Ferrand. Dito isso, como se obtém uma prescrição de cannabis medicinal na França?
Sommaire
ToggleE onde se deve procurar ajuda? Essas são duas perguntas que muitas pessoas estão fazendo. O que, na nossa opinião, é perfeitamente normal. Afinal, a cannabis, seus derivados, sua posse e uso são regulamentados. Portanto, nosso objetivo neste artigo é fornecer informações que possam esclarecer esse assunto.
- Sumário
- Informações sobre pacientes, indicações terapêuticas e prescrições
- Foco nos produtos e seus fornecedores
Segurança do produto
Foco nos centros de referência Informações sobre pacientes, indicações terapêuticas e prescrições Não vamos nos precipitar! De fato, como esta é uma novidade na França, você certamente está se perguntando quantos pacientes estão envolvidos, pelo menos inicialmente. O CBD.FR também se fez essa pergunta. Nesse sentido, nossa pesquisa indica que o programa de testes com cannabis medicinal na França envolverá 3.000 pacientes ao longo de um período de dois anos. Isso é resultado de audiências realizadas pela ANSM (Agência Nacional Francesa de Segurança de Medicamentos e Produtos de Saúde) para estabelecer os parâmetros do programa. É importante ressaltar que, para serem aceitos no programa, os pacientes devem ter tentado diversos tratamentos convencionais sem sucesso e não devem apresentar contraindicações.
Além disso, não foi especificado limite de idade. No entanto, esses pacientes não poderão dirigir durante o período de dois anos do programa. Por quê? Porque alguns medicamentos contêm THC. Ademais, quais são as indicações terapêuticas? Em outras palavras, quais doenças/condições foram selecionadas para este programa de testes com cannabis medicinal na França?
- Na verdade, um total de cinco (5) condições foram selecionadas pelo comitê científico. São elas:
- Espasticidade dolorosa associada a distúrbios do sistema nervoso central.
- Certas formas graves e resistentes a medicamentos de epilepsia.
- Situações de cuidados paliativos.
- Certos sintomas refratários em oncologia.
Dor neuropática que não responde aos tratamentos disponíveis.
Além disso, como funcionarão as prescrições para os pacientes em questão? Dois pontos são essenciais a esse respeito. Primeiro, as prescrições devem ser emitidas por médicos especialistas nessas condições. Segundo, os pacientes, com suas prescrições, devem retirar seus produtos à base de cannabis nas farmácias. Foco nos produtos e seus fornecedores
Na verdade, certas formas de cannabis foram selecionadas. Estas incluem, entre outras, óleo, flores e formas orais. Nesse sentido, as proporções relevantes são as seguintes: predominância de THC, predominância de CBD ou uma proporção equilibrada de THC/CBD. A esse respeito, a ANSM (Agência Nacional Francesa de Segurança de Medicamentos e Produtos de Saúde) desaconselha o consumo de flores na forma de cigarros. Em vez disso, recomenda-se o uso em infusões.E quanto aos fornecedores? Como todos sabemos, o cultivo de cannabis medicinal ainda é proibido na França. Consequentemente, a ANSM selecionou empresas estrangeiras para fornecer os produtos necessários para o ensaio clínico com cannabis medicinal na França. Essas empresas fornecerão os produtos gratuitamente durante a duração do programa.
Uma nota sobre a segurança dos produtos: Os responsáveis pelo programa estão garantindo que todos os produtos utilizados sejam seguros para os pacientes. Nesse sentido, dois lotes de medicamentos já foram recolhidos devido a defeitos de fabricação. A ANSM abordou essa questão em um comunicado à imprensa datado de 2 de abril.
“Diversos incidentes foram relatados à ANSM (Agência Nacional Francesa de Segurança de Medicamentos e Produtos de Saúde) referentes a um defeito de qualidade na solução oral Tilray THC10 CBD10. Esse defeito envolve um vazamento na tampa do frasco. A Medipha, empresa que comercializa este medicamento para a Tilray, está recolhendo os lotes afetados, que foram colocados em quarentena até o término do recolhimento. Nenhum frasco foi dispensado a pacientes. Médicos e farmacêuticos participantes do estudo clínico foram informados de que não devem mais prescrever ou dispensar os lotes afetados pelo recolhimento. Outros medicamentos disponíveis permitem que o estudo clínico continue e garantam que as necessidades dos pacientes sejam atendidas.”
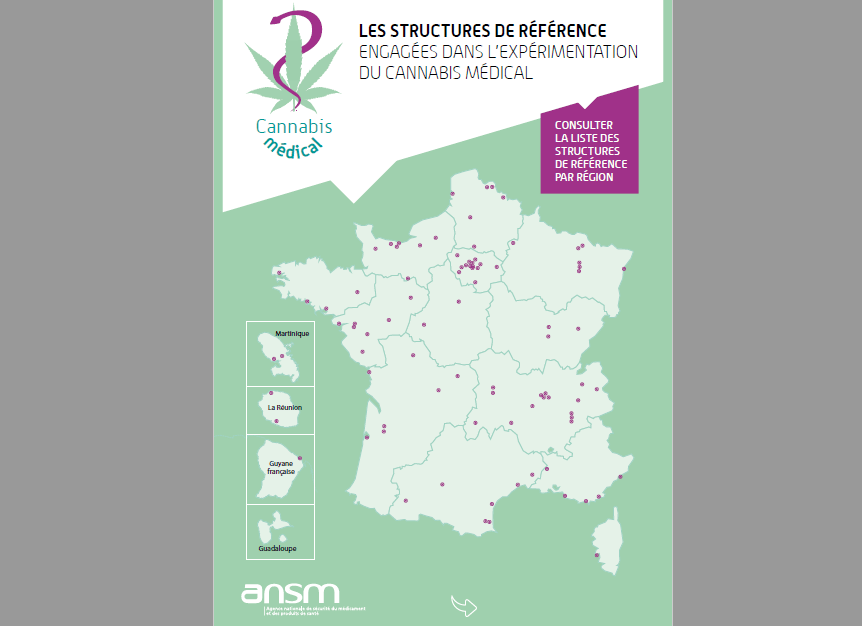
Foco nos Centros de Referência Uma lista de 200 centros de referência localizados em 170 hospitais foi publicada para facilitar o acesso dos pacientes participantes deste programa.
O CBD.FR
também disponibiliza esta lista aos seus leitores. Você pode visualizar o mapa interativo completo dos centros de referência abaixo. Caso seu dispositivo não permita, convidamos você a baixar sua cópia para sua conveniência. Deseja baixar sua cópia? Faça isso abaixo! Leia também: