L’expérimentation du cannabis thérapeutique a enfin commencé. À ce sujet, le vendredi 26 mars 2021, la plante médicale a été prescrite pour la première fois au CHU de Clermont-Ferrand. Ceci dit, comment se faire prescrire du cannabis médical en France ? Et de quel côté se rendre ? Deux questions que nombre de personnes se posent. Ce qui, en notre sens, est tout à fait normal. Parce que le cannabis, ses dérivés, leurs possession et usage sont régulés. Nous nous proposons donc de vous fournir des informations susceptibles de vous éclairer sur ce sujet dans cet article.
Sommaire
ToggleLe sommaire
- Informations sur les patients, les indications thérapeutiques et les prescriptions
- Focus sur les produits et leurs fournisseurs
- Point sur la sécurité des produits
- Focus sur les structures référentes
Informations sur les patients, les indications thérapeutiques et les prescriptions
Ne sautons pas les étapes ! En effet, ceci étant une première en France, vous vous demandez certainement le nombre de patients qui sont concernés, pour un début. CBD.FR s’est également posé cette question. À ce sujet, après nos recherches, il s’avère que le programme d’expérimentation du cannabis médical en France concernera 3000 patients pour une période de deux ans. Cela est une résultante des auditions menées par l’ANSM afin d’en fixer les modalités. Il est important de savoir que pour être accepté dans le programme, le patient doit avoir déjà testé plusieurs traitements classiques, sans succès et ne pas présenter de contre-indication.
Aussi, aucune limite d’âge n’a été spécifiée. Par contre, ces patients n’auront pas le droit de conduire pendant les deux ans d’expérimentation. Pourquoi ? Parce que certains médicaments contiennent du THC.
Par ailleurs, qu’en est-il des indications thérapeutiques ? Dit, autrement, quelles sont les maladies / pathologies sélectionnées pour cette expérimentation du cannabis médical en France ? En fait, au total (05) cinq ont été retenues par le comité scientifique. Il s’agit de :
- Spasticités douloureuses des pathologies du système nerveux central.
- Certaines formes d’épilepsie sévères et pharmaco-résistantes.
- Situations palliatives.
- Certains symptômes rebelles en oncologie.
- Douleurs neuropathiques réfractaires aux thérapeutiques accessibles.
En outre, comment fonctionneront les prescriptions pour les patients concernés ? En effet, deux points sont essentiels pour cet aspect. D’une part, les prescriptions devront être faites par les médecins spécialistes de ces pathologies. D’autre part, les patients munis de leur ordonnance devront ensuite aller récupérer leurs produits à base de cannabis dans les pharmacies.
Focus sur les produits et leurs fournisseurs
De fait, certaines formes du cannabis ont été retenues. Il s’agit, en autres, de l’huile, des fleurs et formes orales. À ce sujet, les ratios y afférents sont les suivants : dominant THC, dominant CBD, ou ratio équilibré THC / CBD. Allant dans ce sens, l’ANSM déconseille la consommation des fleurs sous forme de joints. Mais, recommande plutôt de le faire en infusions.
Que dire sur les fournisseurs ? En fait, comme nous le savons tous, la culture du cannabis thérapeutique est encore interdite en France. En conséquence, l’ANSM a sélectionné des entreprises étrangères pour fournir les produits nécessaires à l’expérimentation du cannabis médical en France. Celles-ci (lesdites entreprises) fourniront les produits gratuitement durant toute la durée du programme.
Point sur la sécurité des produits
En effet, les dirigeants de ce programme veillent à ce que tous les produits utilisés soient sûrs pour les patients. À ce sujet, deux lots de médicaments ont déjà été rappelés pour défaut de fabrication. Sous cet angle, l’ANSM, dans un communiqué du 2 avril, s’exprime.
« Plusieurs déclarations d’incidents ont été rapportées à l’ANSM concernant un défaut qualité du médicament Tilray Solution Orale THC10 CBD10. Ce défaut qualité correspond à une fuite au niveau du bouchon du flacon. La société Medipha, exploitant de ce médicament pour la société Tilray, procède à un rappel des lots concernés qui ont été mis en quarantaine dans cette attente. Aucun flacon n’a été délivré à aucun patient. Les médecins et les pharmaciens participant à l’expérimentation ont été informés qu’ils ne doivent plus prescrire ni délivrer les lots concernés par le rappel. Les autres médicaments disponibles permettent de poursuivre l’expérimentation et de garantir la couverture des besoins des patients. »
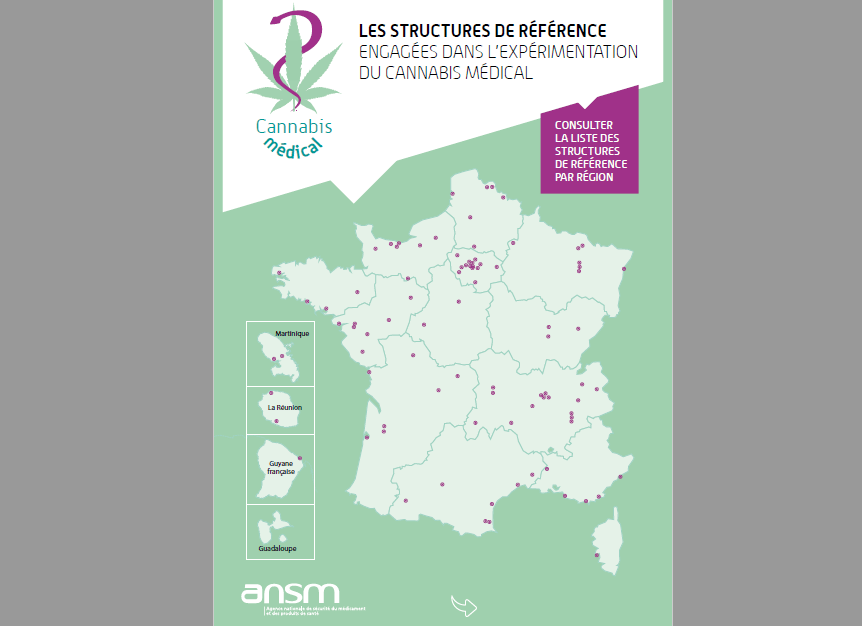
Focus sur les structures référentes
Une liste de 200 centres de références repartis dans 170 hôpitaux a été publiée pour faciliter la vie aux patients concernés par ce programme. CBD.FR de son côté, la rend également accessible pour ses lecteurs. Vous pouvez consulter l’intégralité de la carte interactive des structures de référence ci-dessous. Si votre appareil ne vous le permet pas, nous vous invitons à télécharger votre exemplaire pour plus de confort.
Vous souhaitez télécharger votre exemplaire ? Faites-le ci-dessous !
À lire également : Publication du décret autorisant l’expérimentation du Cannabis thérapeutique en France.
Rédacteur en chef spécialisé en CBD
Julien, né le 17 juillet 1978 en région Parisienne, est un éminent rédacteur et expert dans le domaine des produits à base de CBD. Suite à ses études, Julien a développé une passion pour les remèdes naturels, dont le CBD. En 2022, il intègre l’équipe du site CBD.fr en qualité d’expert et de contributeur régulier. Grâce à son expertise scientifique et une écriture claire, Julien aide à démystifier les aspects complexes du CBD, tout en mettant en lumière ses bienfaits et applications potentielles à travers ses articles et participations à des conférences.